Od „fabryki superświatła” po badania interdyscyplinarne
Lata czterdzieste XX wieku. W wielu laboratoriach naukowych prowadzone są badania z zakresu fizyki jądrowej (dla przypomnienia: materia składa się z cząsteczek; cząsteczki zbudowane są z atomów; atom to w przybliżeniu małe, ciężkie jądro atomowe złożone z protonów i neutronów oraz krążące dookoła niego po orbitach elektrony). Oddzielone od jądra elektrony przyspieszane są do bardzo dużych prędkości, bliskich prędkości światła. Przyspieszanie do tak dużych prędkości wymaga długiego toru, więc aby nie zajmować nieskończonego obszaru, najłatwiej realizować to w przyspieszaczu o kształcie kołowym. Spróbujmy sobie wyobrazić elektron jako człowieka biegnącego po okręgu z masą rzeczy do przeniesienia. Biegnąc i stale przyśpieszając, na zakręcie gubi cześć rzeczy, które nabierają prędkości.
Zjawisko to nie wydaje się być korzystne i wówczas myślano podobnie. Przewidywano istnienie promieniowania, które będzie emitowane w momencie, gdy przyspieszany elektron będzie zakręcał, poruszając się po swoim torze. W związku z tym próbowano budować urządzenia, w których ta emisja byłaby minimalna (minimalna strata prędkości elektronu). Okazało się jednak, że zaproponowane rozwiązania nie do końca się sprawdzały. Za to udało się coś innego! 24 kwietnia 1947 roku po raz pierwszy zaobserwowano promieniowanie, którego istnienie wcześniej przewidywała jedynie teoria.
Właściwie na tym można by zaprzestać prowadzenia dalszych badań. Naukowcy poszli jednak dalej, postanowili zbadać to promieniowanie i stwierdzili, że ma ono niezwykłe własności. Jego wiązka jest bardzo intensywna, ma szeroki zakres energii (długości fali) oraz jest niezwykle dobrze zogniskowana (bez użycia dodatkowych systemów). Promieniowanie to uznano za „superświatło” i nazwano promieniowaniem synchrotronowym. W nadziei na jego wykorzystanie naukowcy przestali uważać to zjawisko za pasożytnicze i zaczęli budować urządzenia do jego wytwarzania. Wielkie przyspieszacze kołowe, zwane synchrotronami, zostały przeznaczone do wytwarzania takiego promieniowania – rozpoczęła się era „fabryk superświatła”.
Wchodzimy w mikroświat
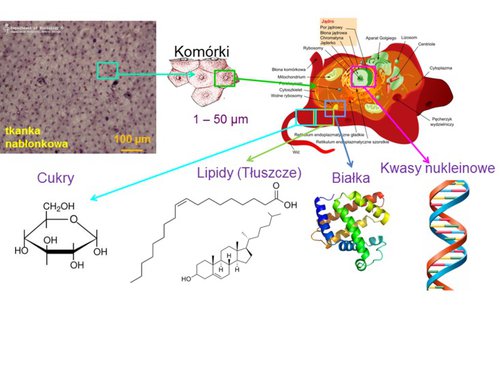
Wyobraźmy sobie system złożony. Jako przykład weźmy układ biologiczny – fragment tkanki (np. skóry). Używając znanego ze szkoły mikroskopu optycznego i zmieniając powiększenie, dostrzegamy kolejno, że tkanka złożona jest z komórek, które mają rozmiar rzędu mikrometrów (1 mikrometr = 10‑6 m; jedna milionowa cześć metra) oraz że komórki posiadają różne organella komórkowe. Na tym jednak zakres mikroskopii optycznej właściwie się kończy – jesteśmy w stanie dostrzec obiekty powiększone do rozmiarów kilkuset nanometrów (1 nanometr = 10-9 m; jedna miliardowa część metra). Ze szkoły wiemy jednak, że różne elementy komórkowe zbudowane są z makrocząsteczek (makromolekuł, biocząstek). Tymi cząstkami mogą być: białka, tłuszcze, cukry, kwasy nukleinowe czy też składniki mineralne (rys. 1). W XXI wieku wiemy również, że m.in. zmiany w ilości i strukturze tych makromolekuł mają wpływ na funkcjonowanie całej komórki, a zbiór komórek o podobnej budowie i pełniących podobne funkcje to właśnie tkanka, budująca nasze organy.
Do badania takich układów potrzebujemy lepszego narzędzia niż tradycyjny mikroskop optyczny (ze światłem widzialnym). Potrzebujemy aparatu, działającego dzięki innemu „rodzajowi” światła, które powinno: być intensywne, aby móc badać obiekty występujące w małych stężeniach (np. kwasy nukleinowe w komórce); mieć małych rozmiarów wiązkę, aby móc badać niewielkie obiekty; być łatwo przestrajalne, aby zmieniając energię (długość fali) można było badać różne struktury i właściwości danego obiektu.
Odkryte w XX wieku promieniowanie synchrotronowe w pełni spełnia postawione warunki.
Myślimy interdyscyplinarnie
W 2009 roku rozpoczęłam współpracę z Katedrą Histologii Collegium Medicum Uniwersytetu Jagiellońskiego, gdzie poznałam doktora nauk medycznych zajmującego się barwieniem tkanek. Polega ono na tym, że używając odpowiedniego czynnika chemicznego uwrażliwia się konkretne elementy komórkowe lub cząsteczki na światło, którym oświetla się preparat pod mikroskopem dając obraz obecności poszukiwanych struktur. Badania takie są bardzo ciekawe i często wykorzystywane w diagnostyce do oceny np. zmian patologicznych w materiale pobranym podczas biopsji. Niestety, użycie jednego barwnika wyklucza użycie innego na tym samym skrawku tkanki. Zadaliśmy sobie pytanie, czy możliwe jest wykorzystanie metod współczesnej fizyki, aby wspomóc badania nad chorobami.
W sferze zainteresowań biomedyków jest np. rola pierwiastków śladowych (występujących poniżej 1% w organizmie) w mechanizmie chorobotwórczym czy też zmiany zachodzące w makromolekułach w czasie rozwoju choroby. Wspomniany doktor pracował nad badaniem wpływu diet oraz leków na przebieg miażdżycy. Jest to choroba, w której dochodzi do odkładania się różnych substancji w tętnicach, co prowadzi do ich zwężenia, a w konsekwencji – zatkania. To bardzo niebezpieczny proces, bo może skutkować zawałem serca czy udarem mózgu. Naukowcom udało się wynaleźć leki, które przy wczesnym wykryciu choroby pomagają w kontrolowaniu jej przebiegu, ale do tej pory nie są znane przyczyny jej powstawania, jak i przebieg jej początkowego mechanizmu. Wiele grup badawczych na świecie próbuje badać patomechanizm tej choroby. Postuluje się m.in. udział pierwiastków śladowych, głównie tych, które związane są z makromolekułami (żelazo, miedź, cynk) w rozwoju miażdżycy. Co więcej, zaobserwowano odkładanie soli wapniowych i fosforanowych jako tzw. płytek miażdżycowych w późnym etapie choroby, które nie przepuszczają krążącej w organizmie krwi oraz elementów odżywczych w niej zawartych. Wiadomo również, że w pierwszym okresie rozwoju choroby dochodzi w tętnicach do akumulacji tłuszczy, obecnych w krążącej krwi. Postawiliśmy sobie za cel próbę określenia, czy te składniki chemiczne rzeczywiście związane są z rozwojem choroby. W naszym pionierskim eksperymencie wykorzystaliśmy myszy z wywołaną genetycznie miażdżycą. Jedna grupa (kontrolna) karmiona była normalną paszą i niepoddawana żadnym innym środkom odżywczym. Druga grupa (eksperymentalna) wraz z pożywieniem otrzymywała dodatkowo nowy, eksperymentalny lek o nazwie AVE – 0991.
W tego typu badaniach potrzebny jest jedynie cienki skrawek tkanki (kilka mikrometrów), dlatego w naszej analizie skupiliśmy się głównie na aorcie (największej tętnicy), a dokładniej mówiąc – na jej przekroju poprzecznym.
Pomiary, pomiary…
Zaproponowałam dwie metody spektroskopowe wykorzystujące „superświatło”, oparte na analizie oddziaływania promieniowania z materią. Aby badać zawartość pierwiastków śladowych bądź makromolekuł, potrzebujemy różnych długości fali, czyli tak naprawdę dwóch różnych „własności” naszej wiązki próbkującej. W pierwszym przypadku potrzebujemy dużo więcej energii niż w drugim.
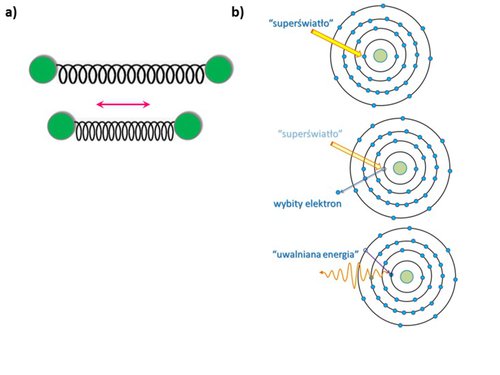
Wyobraźmy sobie dwa atomy połączone ze sobą wiązaniem chemicznym, które jest dość „elastyczne”, dlatego można je przedstawić za pomocą sprężynki (rys. 2a). Aby atomy zaczęły drgać, odpowiednio skracając i wydłużając sprężynkę, musimy dostarczyć pewnej porcji energii. Taki układ w zależności od wzajemnego położenia atomów wobec siebie („długości sprężynki”) zmienia swoją energię. Właśnie zmianę tej energii mierzymy w eksperymencie spektroskopowym, o którym mówimy, że odbywa się w zakresie energii podczerwieni. Energia, jaką posiada układ atomów, zależy od masy atomów, od „długości” wiązania oraz od liczby atomów i wiązań między nimi. W zależności od tego, z jakim układem mamy do czynienia i w jaki sposób on drga, taką wartość zmiany energii otrzymujemy w eksperymencie. Ponadto, zależnie od liczby podobnych układów atomów w danej próbce, zmierzymy odpowiednio dużo lub mało porcji tej energii. Na tej podstawie możemy określić, z jakimi i iloma grupami charakterystycznymi dla makromolekuł mamy do czynienia. Jeżeli natomiast, zamiast wzbudzać atomy do drgania względem siebie, będziemy chcieli zmienić stan samego atomu, można to zrobić poprzez oddziaływanie promieniowania z elektronem. Możemy np. użyć naszego „superświatła” do wybicia elektronu z orbity wokół jądra. Atom „nie lubi” zmieniać swojego stanu, w szczególności dotyczy to elektronu z powłoki położonej blisko jądra. Dlatego w takim przypadku elektron z dalszej powłoki zapełnia dziurę po wybitym elektronie. Drugi elektron, znajdujący się dalej od jądra, musi mieć większą energię, aby utrzymać się w atomie, więc przechodząc do stanu niżejenergetycznego emituje porcję energii, która jest przez nas mierzona. Ilość porcji tej energii oraz jej wartość mówi nam o tym, z jakim pierwiastkiem mamy do czynienia (rys. 2b). Mówimy wtedy o spektroskopii promieniowania X.
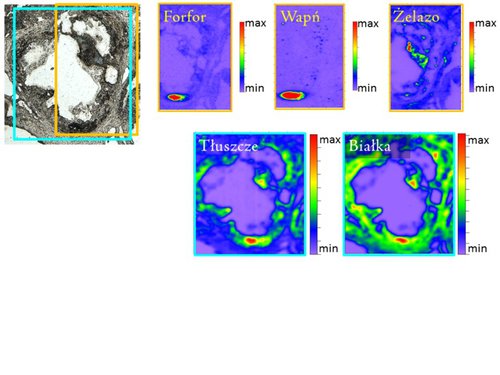
Wiązka promieniowania synchrotronowego ma tę własność, że sama w sobie jest zogniskowana, a więc jest niedużych rozmiarów, co umożliwia dokładne badanie nawet bardzo małych obszarów próbki. Jeżeli więc w polu widzenia wiązki umieścimy naszą próbkę i będziemy ją przesuwać w pionie oraz w poziomie, możemy uzyskać dane odnośnie do składu i rozmieszczenia zarówno biocząstek, jak i pierwiastków z każdego punktu próbki. Jeżeli odpowiedniej ilości zmierzonych porcji energii przypiszemy skale kolorów, to możemy uzyskać dwuwymiarowe mapy ich rozkładu, jak przykładowo pokazano na rysunku 3.
Jak już wspomniałam, synchrotrony są dużymi, zaawansowanymi urządzeniami badawczymi, ale również same układy eksperymentalne są skomplikowane. Często stacje końcowe wyposażone są w wiele elementów, które współdziałają ze sobą podczas pomiarów w celu uzyskania pożądanych informacji o badanym układzie. Pomiary na takich liniach doświadczalnych wymagają nieraz dużo czasu i wysiłku.
Wpływ leku, czyli parę słów o wynikach
Dokonanie wspomnianych pomiarów (w „fabrykach superświatła” w Niemczech i Francji) oraz uzyskanie pokazanych map zajęło nam sporo czasu. Otrzymaliśmy rozkłady chemiczne w badanych próbkach, ale pozostaje pytanie, co z nich wynika. Przede wszystkim na obrazkach widzimy charakterystyczne skupienia, w których występuje dużo więcej wapnia i fosforu. Są to miejsca, gdzie rozwój miażdżycy jest daleko posunięty i tworzą się tzw. płytki miażdżycowe w postaci soli wapniowo-fosforanowych. Ponadto na uzyskanych obrazach widać, że więcej żelaza odkłada się wewnątrz światła aorty. Związane jest to z przepływem krwi zawierającej hemoglobinę, w skład której wchodzi żelazo.
Przejdźmy dalej do makromolekuł: tłuszcze występują bardziej wewnętrznie, a białka na zewnątrz przekroju tętnicy. Nic dziwnego, tłuszcze akumulują się w miejscu uszkodzenia aorty, przy przepływie z krwią, a białka są składnikami budującymi ścianę aorty. To wiemy, a czy wyniki mówią coś więcej? A jakże! Możemy porównać zawartości poszczególnych pierwiastków i biocząstek między grupą kontrolną i leczoną. Takie zestawienie pokazuje, że w grupie leczonej ilość zarówno wapnia, jak i fosforu w płytkach miażdżycowych jest mniejsza, co wskazuje na korzystne działanie leku. W tej grupie obserwujemy również większe zawartości żelaza, prawdopodobnie ze względu na mniejsze uszkodzenia tętnicy i lepszy przepływ krwi.
A co z biocząstkami w obu grupach? W grupie kontrolnej rozkład tłuszczy jest pasmowy, podczas gdy w grupie leczonej występuje bardziej punktowe rozłożenie. Świadczy to o mniejszym zaawansowaniu choroby lub jej regresji pod wpływem leku. Ponadto bardziej równomierne rozłożenie ugrupowań białkowych świadczy o lepszym stanie samej ściany tętniczej.
Dalsze analizy uzyskanych wyników pozwolą na wyciągniecie kolejnych wniosków na temat wpływu leków i diet na rozwój bądź zahamowanie choroby, co przybliży nas do poznania jej mechanizmu. Warte podkreślenia jest to, że pomiary dwoma metodami udało się wykonać na jednym skrawku próbki oraz że zawartości wszystkich pierwiastków określono na podstawie pojedynczego pomiaru, podobnie jak biomolekuł. Współpraca obu środowisk przynosi wymierne efekty w dążeniu do poznania patomechanizmów choroby i określenia odpowiedniego leczenia.


Komentarze
Tylko artykuły z ostatnich 12 miesięcy mogą być komentowane.